Состав химического стекла: Из чего делают стекло. Виды, способы изготовления стекла ☑️ EraGlass
- Химический состав и свойства электроламповых стекол | Производство источников света
- Из чего делают стекло. Виды, способы изготовления стекла ☑️ EraGlass — Мир Окон 🏠
- стеклянных материалов | Текущий
- Все о натриево-известковом стекле – Состав и свойства – Передовые технические продукты
Химический состав и свойства электроламповых стекол | Производство источников света
Сторінка 8 із 67
б) Химический состав и свойства электроламповых стекол.
В производстве источников света широко используются 15—20 наименований стекол. Все они, за исключением кварцевого стекла, многокомпонентные, т. е. в их состав входят три или более различных окислов. Это позволяет изменять в широких пределах свойства стекол. Химический состав основных электроламповых стекол приведен в табл. 1.5.
Входящие в стекло окислы разделяются на следующие группы:
- кислотные и стеклообразующие SiO2, В2O3, Р2О5, которые служат основой стекла и без одного из них стекло не может образовываться;
- щелочные Na2O и К2O, которые понижают температуру варки и размягчения стекла, уменьшают вязкость и твердость, понижают термическую и химическую стойкость, уменьшают склонность стекла к кристаллизации, повышают электропроводность и температурный коэффициент линейного расширения; .

- щелочноземельные СаО и MgO, которые ослабляют некоторые отрицательные свойства, придаваемые стеклу окислами первых двух групп;
- окислы тяжелых металлов РЬО и ВаО, которые повышают плотность стекла, придают стеклу блеск, улучшают его электроизоляционные свойства, понижают вязкость и твердость.
Помимо того, в состав стекла для придания ему специфических свойств могут вводиться и другие окислы — алюминия, цинка и т. д.
Некоторые важнейшие свойства электроламповых стекол приведены в табл. 1.6.
Механические свойства.
Стекла отличаются малой прочностью при растяжении и сравнительно большой прочностью на сжатие. Предел прочности при растяжении отожженных стекол колеблется от 35 до 1250 МПа. Механическая прочность стекол повышается при увеличении содержания в нем двуокиси кремния, окислов кальция, бария и бора и уменьшается при увеличении содержания окислов свинца, натрия и калия. Однако прочность стекла больше зависит от размеров, формы, состояния поверхности и режима термической обработки (наличия напряжений), чем от химического состава.
Таблица 1.5. Химический состав стекол
Поэтому специальное повышение механической прочности, т. е. упрочнение стекла, может быть получено несколькими способами; тщательным отжигом, огневой полировкой поверхности, стравливанием поверхностного слоя, нанесением на поверхность стекла за щитных пленок, созданием в поверхностном слое равномерного напряжения путем ионного обмена из газовой или жидкой среды, а также конструктивными приемами.
Твердость электроламповых стекол колеблется в пределах 4—7 единиц по десятибалльной шкале Мооса. Наиболее твердыми являются кварцевое и вольфрамовые стекла, наименее твердыми — свинцовые.
Стекло плохо переносит динамические нагрузки (удары), т. е. оно хрупко. Особенно сильно хрупкость стекла повышается при наличии на его поверхности или в толще микротрещин, напряжений.
Химические свойства.
При производстве источников света и их последующем использовании большое значение имеет стойкость стекол к действию кислот, щелочей, паров некоторых металлов, влаги.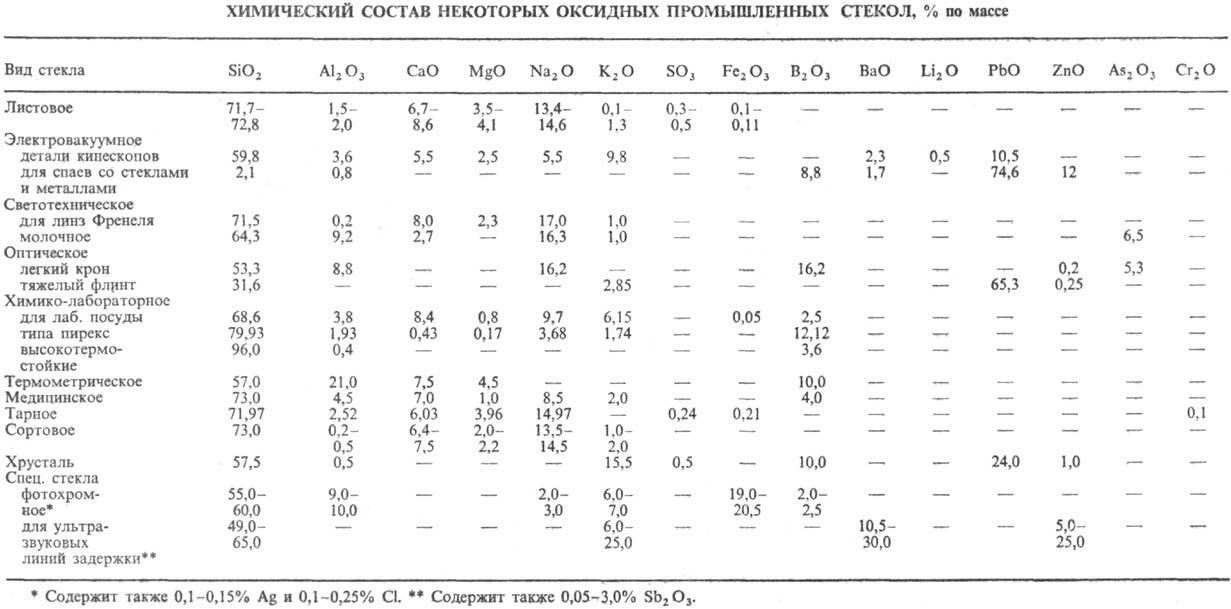 К действию большинства кислот стекла, как правило, стойки. Только фосфорная и плавиковая кислоты оказывают на стекла сильное воздействие. Это используется для матирования и очистки силикатных и боросиликатных стекол.
К действию большинства кислот стекла, как правило, стойки. Только фосфорная и плавиковая кислоты оказывают на стекла сильное воздействие. Это используется для матирования и очистки силикатных и боросиликатных стекол.
По отношению к щелочам большинство стекол мало стойки. Обычные силикатные стекла нестойки к действию паров щелочных и щелочноземельных металлов. Поэтому в натриевых, цезиевых и некоторых других газоразрядных лампах с парами указанных металлов применяются специальные стекла с нулевым или очень малым содержанием двуокиси кремния.
Под действием влаги стекло способно разрушаться («выветриваться»). При этом происходит гидролиз входящих в состав стекла силикатов щелочных металлов. В результате на поверхности стекла появляются трудно удалимые мутные разводы, стекло тускнеет, теряет прозрачность. При нагревании в пламени газовой горелки «выветренное» стекло еще более мутнеет и кристаллизуется. Качество стеклоизделий резко ухудшается. Иногда удается «выветренное» стекло восстановить путем стравливания поверхностного слоя с помощью плавиковой кислоты.
Хорошо защищают стекло от воздействия влаги при хранении гидрофобные кремний-органические покрытия и парафинированная бумага. Стекла, прошедшие огневую обработку, становятся более устойчивыми.
Химическая стойкость стекла определяется в первую очередь его химическим составом. Все стекла по химической стойкости подразделяются на пять гидролитических классов. Наиболее стойкие стекла относят к первому классу, а наименее стойкие — к пятому.
Термические свойства.
Важнейшими термическими свойствами стекла являются теплоемкость, теплопроводность, температурный коэффициент линейного расширения (ТКЛР), стойкость к термоударам и температура размягчения.
Таблица 1.6. Физико-химические свойства и применение электроламповых стекол
Стекла обладают малой удельной теплоемкостью — от 400 до 1000 Дж/(кг-К) и малой теплопроводностью — 3 от 0,7 до 1,3 Вт/(м-К). Теплоемкость имеет значение как фактор, определяющий затраты теплоты на нагрев стекла при его обработке, скорость нагрева и охлаждения. Малая же теплопроводность Стекла является основной причиной неравномерного охлаждения стекла и возникновения в стекле внутренних напряжений.
Малая же теплопроводность Стекла является основной причиной неравномерного охлаждения стекла и возникновения в стекле внутренних напряжений.
Температурный коэффициент линейного расширения (ТКЛР) показывает относительное приращение длины стеклянного образца при его нагреве на один кельвин:
где l — первоначальная длина образца, мм; Δl — приращение длины образца при нагреве, мм; ΔΤ — приращение температуры, К.
От ТКЛР зависит прочность спаев стекол, а также стойкость стекла к резким переменам температур. Он определяется химическим составом стекла. Окислы калия и натрия увеличивают ТКЛР, а двуокись кремния, окислы магния, алюминия и бора — уменьшают его.
В условном обозначении марки стекла указывают значение ТКЛР, измеренное на дилатометрах типа ДКВ, усредненное в интервале температур 20—300 °C и уменьшенное в 107 раз. В производственных условиях ТКЛР обычно контролируется не реже 1 раза в месяц дилатометрическим методом и ежедневно — методом двойной нити по ОСТ 16. 0649.001-74.
0649.001-74.
Соединение стекол между собой, а также с другими материалами требует знания усредненного значения ТКЛР и его зависимости от изменения температуры.
Стойкость к термоударам — это способность стекла выдерживать максимальные изменения температур без разрушения. Стойкость стекла к термоударам характеризует допустимую скорость охлаждения и нагрева стеклянных деталей и спаев в процессе их производства и эксплуатации. Для большинства электроламповых стекол стойкость их к термоударам (термостойкость) находится в пределах от 120 до 280 °C. Стандартные испытания производятся на стеклянных стержнях определенного размера с оплавленными концами, которые подвергаются соответствующему прогреву и затем погружаются в воду.
Двуокись кремния, окислы алюминия и бора увеличивают термостойкость стекла, а окислы щелочных металлов — понижают. Изделия, имеющие посторонние включения в стекле, большую толщину стенок, резкие переходы от одной толщины к другой, дефекты на поверхности стекла, внутренние напряжения, обладают пониженной термостойкостью. Можно считать, что термостойкость прямо пропорциональна механической прочности стекла и обратно пропорциональна его ТКЛР.
Можно считать, что термостойкость прямо пропорциональна механической прочности стекла и обратно пропорциональна его ТКЛР.
Стекло в отличие от кристаллических веществ не имеет определенной температуры плавления. Поэтому для оценки степени тугоплавкости стекла и для характеристики его поведения при огневой обработке введено понятие о температуре размягчения, тесно связанное с понятием вязкости стекла. Температура, при которой стекло начинает деформироваться под действием собственного веса, называется температурой размягчения.
Ввиду большого значения температуры размягчения в производстве электроламповых стекол ее ежедневно контролируют для двух точек, соответствующих вязкости стекла 1010 и 106,65 Па-с. При изменении температуры вязкость стекла может меняться в очень широких пределах. Знание кривой вязкости (см. рис. 1.2) данной марки стекла имеет большое значение для установления оптимальных режимов обработки стекла путем нагрева, а также оценки возможности его применения.
При варке стекла вязкость стекломассы обычно находится в пределах от 1 до 103 Па-с. Вязкость застывающего стекла при комнатной температуре равна примерно 1015 Па-с. В диапазоне вязкости 103—107 Па-с стекло может подвергаться пластическим деформациям. При этом практически вязкость определяют по цвету размягченной части стекла в рабочем состоянии (кварцевое — ослепительно белое, молибденовое — темно-красное с белым свечением и т. д.).
Большое практическое значение имеет скорость изменения вязкости стекла при изменении температуры. В зависимости от температурного интервала пластического состояния различают «длинные» и «короткие» стекла. У длинных стекол этот интервал больше, чем у коротких.
Электроламповые стекла не должны быть слишком длинными или слишком короткими. Изделия из короткого стекла требуют быстрой выработки и обработки на огне. Чем короче стекло, тем труднее выдержать температуру, соответствующую необходимой рабочей вязкости. У длинных стекол небольшие колебания температуры практически не сказываются на вязкости, поэтому изготовление и обработка изделий из такого стекла легко поддается автоматизации. Однако длинные стекла требуют более продолжительного нагрева в начале огневой обработки и более длительного остывания после окончания ее. Вследствие этого уменьшается производительность оборудования.
Однако длинные стекла требуют более продолжительного нагрева в начале огневой обработки и более длительного остывания после окончания ее. Вследствие этого уменьшается производительность оборудования.
Стекла, содержащие значительные количества окислов PbO, Na2O, К2О, ВаО, являются длинными, a SiO2, ZnO, А12O3, MgO — короткими. Одним из наиболее коротких стекол является кварцевое, а одним из наиболее длинных— свинцовое стекло марки СЛ93-1.
Электрические свойства.
При обычных комнатных температурах стекла обладают очень высоким удельным электрическим сопротивлением, которое в зависимости от химического состава имеет значения от 1010 до 1013 Ομ·μ.
Стеклообразующие окислы кремния и бора, а также окислы тяжелых металлов (свинца и бария) улучшают электроизоляционные свойства стекла, а окислы щелочных металлов (натрия и калия)—ухудшают.
С повышением температуры проводимость стекла быстро увеличивается и в интервале 1200—1400 °C стекло становится проводником с ионной проводимостью. При повышенных температурах электрические свойства стекол оцениваются коэффициентом ТК-100, т. е. температурой нагрева стекла, при которой его удельное электрическое сопротивление снизится до 106 Ом-м (100 МОм-см).
При повышенных температурах электрические свойства стекол оцениваются коэффициентом ТК-100, т. е. температурой нагрева стекла, при которой его удельное электрическое сопротивление снизится до 106 Ом-м (100 МОм-см).
Чем выше ТК-100, тем лучше электроизоляционные свойства стекла. Особенно важно иметь большое значение ТК-100 у стекол, используемых для изготовления ножек ламп с большими градиентами потенциала между электродами. Недостаточно высокое значение ТК-100 может в этом случае привести к электролизу стекла ножки между электродами, обусловленному высокой подвижностью ионов лития, натрия и калия. Электролиз особенно опасен в двухсветных автомобильных лампах, имеющих малое расстояние между электродами и высокую температуру ножки (300°C и выше).
Стекло обладает также поверхностной проводимостью, которая во влажной среде может быть больше объемной. Поверхностная проводимость стекол в первую очередь зависит от содержания в стекле щелочных окислов и возрастает при их увеличении. Для устранения поверхностной проводимости стекла обрабатывают гидрофобными веществами (например, парафином, кремний органическими соединениями и т. п.).
Для устранения поверхностной проводимости стекла обрабатывают гидрофобными веществами (например, парафином, кремний органическими соединениями и т. п.).
Напряжение электрического пробоя стекол находится в пределах 20—30 кВ/мм и сильно понижается при увеличении температуры.
Оптические свойства.
Одним из наиболее важных оптических свойств стекла является его прозрачность, т. е. способность пропускать излучения в заданном диапазоне длин волн. Прозрачность стекла в первую очередь определяется его химическим составом. Обычные электроламповые стекла при толщине 1—2 мм поглощают в видимой части спектра от 6 до 20% света. Пониженное пропускание света обусловлено наличием в стекле красителей, вызывающих избирательное поглощение лучей определенной длины волны. Эти красители в стекле часто малозаметны. Например, поглощение света в кажущихся бесцветными, но слабоокрашенных фактически стеклах вызвано присутствием соединений железа. Особенно сильное поглощение видимого излучения вызывается соединениями двухвалентного железа (закисью железа FeO).
Так как для большинства источников света требуется бесцветное стекло, хорошо пропускающее излучение в видимой части спектра, то предпринимаются все меры для его обесцвечивания. С этой целью ограничивают присутствие в стекле закиси железа, проводя химическое и физическое обесцвечивание стекла и тщательно очищая исходные материалы и т. п.
Прозрачность обычных электроламповых стекол сильно уменьшается при переходе в диапазон инфракрасных и ультрафиолетовых излучений. Поэтому для специальных ламп применяют особые стекла, имеющие высокую прозрачность для инфракрасного и ультрафиолетового излучений. Так, колбочное стекло с хорошим пропусканием ультрафиолетового излучения содержит не более 0,006%, примеси железа и большое количество окислов цинка, бора и алюминия.
Часто применяют окрашенные стекла, имеющие избирательное пропускание в нужной части спектра. Окраску производят введением в состав стекла соответствующих окислов. Стекла, содержащие окись хрома, становятся прозрачными для желто-зеленых и темно-красных лучей и интенсивно поглощают синие и фиолетовые. Примесь сульфида кадмия придает стеклу желтую, а примесь окиси кобальта — синюю окраску. Вводя в состав фосфатных стекол окись кобальта или никеля, получают черные увиолевые стекла, хорошо пропускающие ультрафиолетовое излучение и почти полностью поглощающие видимое. Цветное стекло используют в производстве сигнальных и фотоламп, ламп для медицинских целей некоторых газоразрядных источников света.
Примесь сульфида кадмия придает стеклу желтую, а примесь окиси кобальта — синюю окраску. Вводя в состав фосфатных стекол окись кобальта или никеля, получают черные увиолевые стекла, хорошо пропускающие ультрафиолетовое излучение и почти полностью поглощающие видимое. Цветное стекло используют в производстве сигнальных и фотоламп, ламп для медицинских целей некоторых газоразрядных источников света.
Для получения непрозрачных опаловых и молочных стекол в их состав вводят фториды натрия и кальция.
Общее и спектральное пропускание электроламповых стекол может сильно изменяться под действием подающего на них излучения. Этот процесс называется соляризацией стекла. Основной причиной соляризации служит переход под влиянием ультрафиолетового облучения окиси железа в закись. На процесс соляризации влияют также примеси сурьмы, селена, мышьяка и др. Сильно соляризуются мягкие стекла, имеющие в своем составе окислы щелочных металлов. Менее склонны к соляризации стекла с большим содержанием окислов бора, кальция и магния. Установлено, что чем короче длина волны падающего излучения, тем интенсивнее соляризация. Процесс соляризации обратимый: при нагреве стекла до 300—500 °C его прозрачность восстанавливается.
Установлено, что чем короче длина волны падающего излучения, тем интенсивнее соляризация. Процесс соляризации обратимый: при нагреве стекла до 300—500 °C его прозрачность восстанавливается.
Вакуумные свойства.
Важнейшими из вакуумных свойств стекла являются его газопоглощение (и соответственно газоотдача) и газопроницаемость.
После затвердения стекла в нем остается растворенным некоторое количество газов (двуокись углерода, водород, кислород, азот, окись углерода) и паров воды. В 1 г стекла содержится примерно 1—2 см3 газов и паров воды. Основную массу составляют водяные пары. Особенно богата газами и парами поверхность стекла. Толщина поверхностной пленки газов и паров на стекле составляет 50—100 молекулярных слоев и зависит от состава стекла и условий его хранения. Свинцовые и боросиликатные стекла в значительно меньшей степени поглощают газы. Хранение стекла во влажной среде приводит к повышенному растворению в нем газов и паров воды.
Технологический процесс изготовления источников света предусматривает обезгаживание стекла. Хорошее обезгаживание стекла может быть достигнуто его прокалкой в сухом воздухе или в вакууме. Снижение парциального давления вредных газов в стекле можно получить, выдерживая его в атмосфере рабочего газа лампы (например, аргона). Окончательное обезгаживание стекла всегда проводится при вакуумной обработке ламп.
Хорошее обезгаживание стекла может быть достигнуто его прокалкой в сухом воздухе или в вакууме. Снижение парциального давления вредных газов в стекле можно получить, выдерживая его в атмосфере рабочего газа лампы (например, аргона). Окончательное обезгаживание стекла всегда проводится при вакуумной обработке ламп.
Типичная кривая газовыделения стекол при нагревании приведена на рис. 1.3. Основную массу выделяющихся газов ∆Q составляют пары воды и меньшую часть — углекислый газ, кислород, азот и окись углерода.
Первый максимум газовыделения при температуре t1(для мягких стекол 50°C) связан с обильным выделением паров воды с поверхности стекла. По мере истощения этого источника газовыделение уменьшается даже при дальнейшем повышении температуры. Однако, начиная с температуры tmin (350 °C для мягких стекол), количество выделяющихся газов вновь резко возрастает за счет их выделения из объема стекла и начала разложения химических соединений самого стекла. Характер кривых газовыделения сохраняется и для других стекол, меняется только количество газов, состав их и положение максимумов на оси температур.
Рис. 1.3. Кривая газовыделения из стекла
Колбы из окрашенного, матированного или натурального цветного стекла, а также колбы с напыленным слоем вольфрама или другого металла при работе ламп нагреваются до более высоких температур и выделяют поэтому большую массу газов и паров воды, чем колбы из прозрачного бесцветного стекла.
Газопроницаемость большинства электроламповых стекол достаточно мала. Наибольшей способностью проникать через стекло обладает гелий, затем водород. С повышением температуры проницаемость стекол для газов несколько возрастает.
- Попередня
- Наступна
Из чего делают стекло. Виды, способы изготовления стекла ☑️ EraGlass — Мир Окон 🏠
Содержание
Ц.П. Наумов — Химический состав стекла Селитренного городища
К содержанию журнала «Советская археология» (1973, №1)
Лабораторией спектрального анализа ЛОИА АН СССР был исследован материал стеклоделательной мастерской Селитренного городища. Отобранная для анализа часть материала была представлена различными кусочками: отходами производства стекла (семь кусков), стеклом, оставшимся на стенках тиглей и керамики (два образца), бракованными стеклянными изделиями (три образца), полуфабрикатами (одна штука) и готовыми стеклянными изделиями (19 предметов). Всего было выполнено 35 анализов для 32 предметов из стекла. Три стеклянные бусины были проанализированы дважды: для установления химического состава основного тела бусины и для цветного глазка. Изготовленные из цветного стекла бусы и подвески были украшены разноцветными стеклянными глазками и полосками, сочетавшими красный, желтый, зеленый, синий, коричнево-бурый, черный и белый цвета. Весь этот качественно разнообразный материал из стекла представлен двумя химическими типами, которые можно объединить в первоначальный исходный химический тип стекла. Спектральный анализ показал, что все исследованные образцы стекла содержат постоянные главные компоненты, определяющие химический тип, который образован пятью главными компонентами Na20 — CaO — MgO — Al2O3 — SiO2.
Отобранная для анализа часть материала была представлена различными кусочками: отходами производства стекла (семь кусков), стеклом, оставшимся на стенках тиглей и керамики (два образца), бракованными стеклянными изделиями (три образца), полуфабрикатами (одна штука) и готовыми стеклянными изделиями (19 предметов). Всего было выполнено 35 анализов для 32 предметов из стекла. Три стеклянные бусины были проанализированы дважды: для установления химического состава основного тела бусины и для цветного глазка. Изготовленные из цветного стекла бусы и подвески были украшены разноцветными стеклянными глазками и полосками, сочетавшими красный, желтый, зеленый, синий, коричнево-бурый, черный и белый цвета. Весь этот качественно разнообразный материал из стекла представлен двумя химическими типами, которые можно объединить в первоначальный исходный химический тип стекла. Спектральный анализ показал, что все исследованные образцы стекла содержат постоянные главные компоненты, определяющие химический тип, который образован пятью главными компонентами Na20 — CaO — MgO — Al2O3 — SiO2.
Соотношение этих компонентов показывает, что мастера-стеклоделы, по всей видимости, использовали местное сырье — кварцевый песок и золу местных, т. е прикаспийских, растений или морских водорослей, причем кварцевый песок (SiO2) содержал в качестве примесей окислы железа и титана, а также некоторое количество окислов кальция, магния, алюминия, а в состав золы входили окислы натрия, калия, кальция, магния, алюминия и марганца [1]. Стекла, содержавшие набор таких компонентов, в зависимости от условий варки могли быть бесцветными, прозрачными (см. таблицу состава, анализ № 10 — оконный диск) или окрашенными окислами железа и марганца в желто-зеленые и буро-коричневые тона (кусок стекла, анализ № 6, бусина — анализ № 29) [2]. Стекло этого же состава, возможно, содержащее сульфидное
железо, настолько густо окрашивалось, что казалось черным (анализы № 6, 11, 12, 14, 15, 19, 22, 23, 25, 34). Как показало исследование, черное стекло использовалось в качестве основного ядра и служило фоном при производстве глазчатых бус и инкрустированных цветной стеклянной крошкой или полосками.
При производстве однотонных и многоцветных стеклянных украшений, орнаментированных глазками и змейчатыми узорами, применялись красители стекла из свинца и меди. Одновременно с красителем в стекло вводилась двуокись олова, которая делала стекло непрозрачным, глухим. Свинец, добавлявшийся в стекла в виде красителя, в некоторых образцах содержался в таких количествах, что мы были вправе отнести эти стекла к новому химическому типу:
РhО — Na20 — CaO — MgO — А120з — Si02.
Если за условную границу концентрации, определяющую химический тип, считать содержание компонента выше 3%, то из 35 проанализированных стекол 19 относятся к свинцовому типу стекла. Остальные 16 образцов стекла содержали окись свинца в количестве от 2,5% до сотых долей процента и следов. Снижение содержания свинца в стекле в одних случаях можно рассматривать как свинец, использованный в качестве красителя, а в других — как случайную примесь.
В зависимости от условий, при которых проходила варка стекла, свинец и медь образовывали различные химические соединения, которые окрашивали стекла в красный, коричневый, желтый, зеленый и синий цвета. Некоторые из свинцовых стекол содержали такие соединения свинца, которые не были красящими, и стекла оставались бесцветными. К таким относились молочно-белые, заглушенные оловом стекла. Они использовались для получения орнамента в виде полосок и глазков (анализы № 20, 30). Примененное в производстве украшений желтое стекло содержало красящие соединения свинца. Желтое, заглушенное оловом стекло широко применялось
Некоторые из свинцовых стекол содержали такие соединения свинца, которые не были красящими, и стекла оставались бесцветными. К таким относились молочно-белые, заглушенные оловом стекла. Они использовались для получения орнамента в виде полосок и глазков (анализы № 20, 30). Примененное в производстве украшений желтое стекло содержало красящие соединения свинца. Желтое, заглушенное оловом стекло широко применялось
Химический состав стекла Селитренного городища
Продолжение таблицы
при изготовлении однотонных бус и подвесок, при сочетании с другими цветными стеклами составляло элементы глазков и полосок (анализы № 9, 13, 18, 24, 26, 31,32).
Медный краситель в восстановительной среде образует закись меди (Cu20), которая окрашивает стекла в красно-коричневый цвет различной тональности, причем стекла, окрашенные этим соединением меди, становятся непрозрачными и не требуют специального введения двуокиси олова как глушителя. Но тем не менее во всех изученных красных и коричневых стеклах, окрашенных закисью меди, содержалось олово (анализы № 7, 21, 27, 28, 35). Как компонент-глушитель красно-коричневого стекла двуокись олова была лишней. Не исключена вероятность того, что олово вводилось в стекло не самостоятельно, а одновременно со свинцом, находясь в его сплаве. По всей видимости, именно этим и объясняется увеличенное содержание олова в тех стеклах, где больше свинца, и его отсутствие или малое количество в стеклах с низким содержанием свинца.
Как компонент-глушитель красно-коричневого стекла двуокись олова была лишней. Не исключена вероятность того, что олово вводилось в стекло не самостоятельно, а одновременно со свинцом, находясь в его сплаве. По всей видимости, именно этим и объясняется увеличенное содержание олова в тех стеклах, где больше свинца, и его отсутствие или малое количество в стеклах с низким содержанием свинца.
Медный краситель в окислительной среде окрашивает стекла окисью меди (CuO) в голубой и синий цвета (анализы № 1, 4, 5, 8, 17, 33), а в присутствии жел¬того свинцового красителя образуется стекло, окрашенное в зеленый цвет (анализы № 2, 3, 16).
На основании изученного материала стеклоделательной мастерской Селитренного городища можно заключить, что в мастерской производили зольные стекла с постоянным составом пяти компонентов:
Na20 — CaO — MgO — А1203 — Si02.
Свинец, вводимый в стекло указанного состава в качестве красителя, образовывал новый химический тип:
РhО — Na20 — CaO — MgO — А1203 — Si02.
Имея в своем распоряжении в качестве красителей свинец и медь, а также постоянно находящиеся в стекле железо и марганец, стеклоделы так изменяли производственные режимы варки стекла, что могли получать бесцветные прозрачные, стекла и окрашенные в красный, желтый, зеленый, синий, коричневый, черный цвета.
В этот день:
- Дни рождения
- 1802 Родился Поль-Эмиль Ботта — французский дипломат, археолог, натуралист, путешественник, один из первых исследователей Ниневии, Вавилона.
- 1883 Родился Иван Иванович Мещанинов — русский советский лингвист и археолог. Академик Академии наук СССР.
- Дни смерти
- 1978 Умер Сергей Аристархович Семенов — специалист по экспериментальной археологии и первобытной техники, автор методики трасологического анализа первобытных орудий.
- Открытия
- 1876 Генрих Шлиман вскрыл шахтовую гробницу в Микенах с большим количеством золотых вещей — «сокровищами Агамемнона».

- 1912 Людвигом Борхардтом на территории Ахетатона в развалинах мастерской царского скульптора Тутмоса обнаружен лежащий лицом вниз знаменитый скульптурный портрет царицы Нефертити.
Химический состав — стекло — Большая Энциклопедия Нефти и Газа, статья, страница 1
Cтраница 1
| Химическая устойчивость медицинских стекол.
[1] |
Химический состав стекол приведен в табл. 16 главы III настоящего раздела.
[2]
| Химический состав стекол для производства стеклоблоков.
[3] |
Химический состав стекол, В табл. 16 приведен состав стекол для изготовления стеклоблоков.
[4]
| Удельное электросопротивление стеклянных тканей в зависимости от влажности воздуха в ом-см.
[5] |
Химический состав стекла существенно влияет на электрические свойства изделий из стеклянного волокна, особенно на их удельное электросопротивление и диэлектрические потери. С введением окислов щелочных металлов электрические свойства стекла и стеклянных тканей резко снижаются ( табл. 88), особенно заметно при повышении температуры.
С введением окислов щелочных металлов электрические свойства стекла и стеклянных тканей резко снижаются ( табл. 88), особенно заметно при повышении температуры.
[6]
Химический состав стекол в значительной степени влияет на их свойства. Увеличение содержания оксидов А12О3, СаО, ZnO, B2O3, ВаО повышает прочность, твердость, модуль упругости стекла и снижает его хрупкость.
[7]
Химический состав стекла оказывает сильное влияние на основные характеристики стекол: на кристаллизацию стекломассы, вязкость стекла, упругие свойства, термостойкость, а особенно на химическую стойкость и электрические параметры стекол. Прибавление щелочных окислов сильно понижает вязкость стекол и температуру размягчения. В сильной зависимости от химического состава, особенно в условиях нагревания, находятся электрические свойства стекол, так как с повышением температуры в стекле увеличивается подвижность ионов, в особенности одновалентных катионов, и растет электропроводность. Электропроводность повышается также от действия влаги, потому что она является функцией степени электролитической диссоциации и подвижности ионов; при этом доминирующую роль играют катионы щелочных металлов благодаря своим малым размерам.
Электропроводность повышается также от действия влаги, потому что она является функцией степени электролитической диссоциации и подвижности ионов; при этом доминирующую роль играют катионы щелочных металлов благодаря своим малым размерам.
[8]
Химический состав стекла оказывает определенное влияние на величину адгезии, причем степень этого влияния в значительной мере зависит от чистоты поверхности стекла. Поскольку в результате взаимодействия с атмосферной влагой и гидролиза силикатов поверхность всех стекол покрыта тончайшими кремнеземистыми пленками и, кроме того, изменена воздействием агрессивных сред при шлифовании и полировании, то проследить влияние химического состава стекла на объемных образцах стекла почти не удается.
[9]
Химический состав стекла оказывает сильное влияние на основные характеристики стекол: на кристаллизацию стекломассы, вязкость стекла, упругие свойства, термостойкость, а особенно на химическую стойкость и электрические параметры стекол. Прибавление щелочных окислов сильно понижает вязкость стекол и температуру размягчения. В сильной зависимости от химического состава, особенно в условиях нагревания, находятся электрические свойства стекол, так как с повышением температуры в стекле увеличивается подвижность ионов, в особенности одновалентных катионов, и растет электропроводность. Электропроводность повышается также от действия влаги, потому что она является функцией степени электролитической диссоциации и подвижности ионов; при этом доминирующую роль играют катионы щелочных металлов благодаря своим малым размерам.
Прибавление щелочных окислов сильно понижает вязкость стекол и температуру размягчения. В сильной зависимости от химического состава, особенно в условиях нагревания, находятся электрические свойства стекол, так как с повышением температуры в стекле увеличивается подвижность ионов, в особенности одновалентных катионов, и растет электропроводность. Электропроводность повышается также от действия влаги, потому что она является функцией степени электролитической диссоциации и подвижности ионов; при этом доминирующую роль играют катионы щелочных металлов благодаря своим малым размерам.
[10]
Химический состав стекла оказывает определенное влияние на величину адгезии, причем степень этого влияния в значительной мере зависит от чистоты поверхности стекла. Поскольку в результате взаимодействия с атмосферной влагой и гидролиза силикатов поверхность всех стекол покрыта тончайшими кремнеземистыми пленками и, кроме того, изменена воздействием агрессивных сред при шлифовании и полировании, то проследить влияние химического состава стекла на объемных образцах стекла почти не удается.
[11]
Химический состав стекол крайне разнообразен.
[12]
Химический состав стекла включает: силикаты натрия, калия и кальция.
[13]
Химический состав стекла тоже влияет на его механические свойства, но в значительно меньшей степени. Наивысшей прочностью обладают кварцевое и безщелочное стекла. Повышение содержания щелочных окислов Na2O, К2О и окиси свинца понижают прочность стекла; АЬОз, В2Оз, BaO, ZnO, CaO повышают ее.
[14]
Химический состав стекла и метод расчета указаны в § 8 гл.
[15]
Страницы:
1
2
3
4
Боросиликатное стекло: свойства, производство и применение
Боросиликатное стекло, известное своей термостойкостью и физической прочностью, используется во многих областях, в основном связанных с изменениями температуры. Материал обязан своей прочностью и стойкостью уникальному сочетанию кремнезема, оксида бора и других оксидов. Присутствие оксида бора для замены некоторых оксидных компонентов увеличивает силы связывания внутри стеклянного материала.
Присутствие оксида бора для замены некоторых оксидных компонентов увеличивает силы связывания внутри стеклянного материала.
Свойства боросиликатного стекла
Низкое тепловое расширение
Обладая коэффициентом теплового расширения не менее 3,2 x 10 -6 1/K, чистое боросиликатное стекло значительно более устойчиво к изменениям температуры, тогда как другие виды стекла могут деформироваться или деформироваться.
Устойчивость к тепловому удару делает этот материал пригодным для лабораторного обогрева и кухонной посуды. Это характерно низкое тепловое расширение позволяет материалу сохранять свою целостность даже при перемещении из холодного места (например, холодильника) в горячее место (например, духовку) за считанные секунды.
Изменения в количестве его компонентов могут увеличить коэффициент теплового расширения до 7,38 x 10 -6 1/K, но оно по-прежнему гораздо более стойкое, чем обычное известково-натриевое стекло.
Прочие термические свойства боросиликатного стекла включают следующие:
- Температура отжига = 470–640 °C
- Температура размягчения по Вика = 460 — 840°C
- Температура перехода = 440 — 560°C
Высокая прочность материала
По сравнению с аналогичной стеклянной посудой боросиликатное стекло лучше выдерживает удар тупым предметом. Он имеет модуль сдвига 26,5–27 ГПа и твердость по Кнупу 400–480 при 20°C.
Химическая устойчивость
Боросиликатное стекло устойчиво к коррозии и разрушению в кислой среде.
Производство и обработка
Этот особый вид стекла производится путем плавления следующих веществ (с соответствующим приблизительным составом): кварцевый песок (590,5%), оксид бора (21,5%), оксид калия (14,4%), оксид цинка (2,3%) и следовые количества оксида кальция и оксида алюминия.
Другие варианты, например, в случаях, когда боросиликатное стекло используется в качестве посуды, могут изменять состав кремнезема до 81%, в зависимости от его предполагаемого использования.
Процесс плавки требует значительно более высокой температуры, чем традиционное производство стекла, из-за высокой температуры перехода материала до 560°C.
После изготовления подложки боросиликатное стекло можно обрабатывать несколькими способами в зависимости от применения материала. Этот стеклянный материал можно формовать или вытягивать в трубы и обрабатывать до нестандартных форм и размеров.
Применение боросиликатного стекла
Благодаря своим физическим и химическим свойствам боросиликатное стекло нашло применение в самых разных отраслях и областях применения.
Лабораторная стеклянная посуда
Боросиликатное стекло популярно в качестве основного материала для лабораторной посуды, в основном из-за химической и термической стабильности материала. Большинство современных мензурок, колб и других стеклянных сосудов, предназначенных для лабораторного использования, изготовлены из боросиликатного стекла.
Фармацевтические стеклянные трубки
Боросиликатное стекло используется для изготовления фармацевтических контейнеров, таких как шприцы, картриджи, флаконы и ампулы. Материал в основном химически инертен при контакте с большинством жидких лекарственных препаратов.
Материал в основном химически инертен при контакте с большинством жидких лекарственных препаратов.
Посуда и кухонные принадлежности
Благодаря своей исключительной термостойкости этот стеклянный материал нашел применение в кухонной посуде, особенно для приготовления пищи и выпечки. Популярные бренды посуды используют боросиликатное стекло для форм для выпечки и стеклянных кастрюль.
Кроме того, из-за низкого теплового расширения этот стеклянный материал используется для мерных чашек и подобных сосудов. Градация, нанесенная на стеклянную тару, сохраняет свою точность, поскольку материал не деформируется при воздействии высоких температур.
Оптическое оборудование
Благодаря стабильности боросиликатного стекла, это хороший материал для изготовления предметных стекол и линз для микроскопов, телескопов и других оптических устройств. Добавление легирующих добавок может изменить характеристики стекла, такие как спектры оптического поглощения.
Осветительная техника
Осветительному оборудованию требуются стеклянные сосуды и мембраны, способные выдерживать сильный нагрев, и именно здесь боросиликатное стекло чрезвычайно полезно. Устройства, в которых используется этот тип стекла, включают газоразрядные лампы, современные мощные фонари и студийные прожекторы.
Недавние исследования включают модификации химического состава боросиликатного стекла путем добавления легирующих химикатов. Изменение спектров фотолюминесценции материала может стать полезным для твердотельных дисплеев, W-LED и подобных приложений.
Типы и свойства стекла
Стандарты стекла
Изделия из стекла, поставляемые DWK Life Sciences, изготавливаются из различных типов стекла, соответствующих следующим международным стандартам:
| Стандарт | 3.1 Боросиликатное стекло 40100 9000 1.3 Расширение Расширяющее боросиликатное стекло (прозрачное) | 5. 4 Расширяющее боросиликатное стекло (янтарное) | 7. 8 Расширяющее натриево-известковое стекло (янтарное) 8 Расширяющее натриево-известковое стекло (янтарное) | 9.1 Расширяющее натриево-известковое стекло (прозрачное) | |
|---|---|---|---|---|---|
| ASTM E-438 | Тип 1 Класс А | Тип 1 Класс B | Тип 1 Класс B | Тип 2 | Тип 2 |
| Фармакопея США (USP) | Тип 1 | Тип 1 | Тип 1 | Тип 3 | Тип 3 |
| Европейская фармакопея (ЕР) | Тип 1 | Тип 1 | Тип 1 | Тип 3 | Тип 3 |
3.3 Expansion borosilicate glass also complies with ISO 3585 and DIN 12217.
All Pyrex ® , Quickfit ® , SVL ® and many MBL ® and Wheaton ® products are manufactured from 3.3 расширительное боросиликатное стекло (если не указано иное).
Из-за жестких условий, которым подвергается лабораторная стеклянная посуда, максимальная химическая стойкость, минимальное тепловое расширение и высокая устойчивость к тепловому удару являются ключевыми свойствами боросиликатного стекла расширения 3.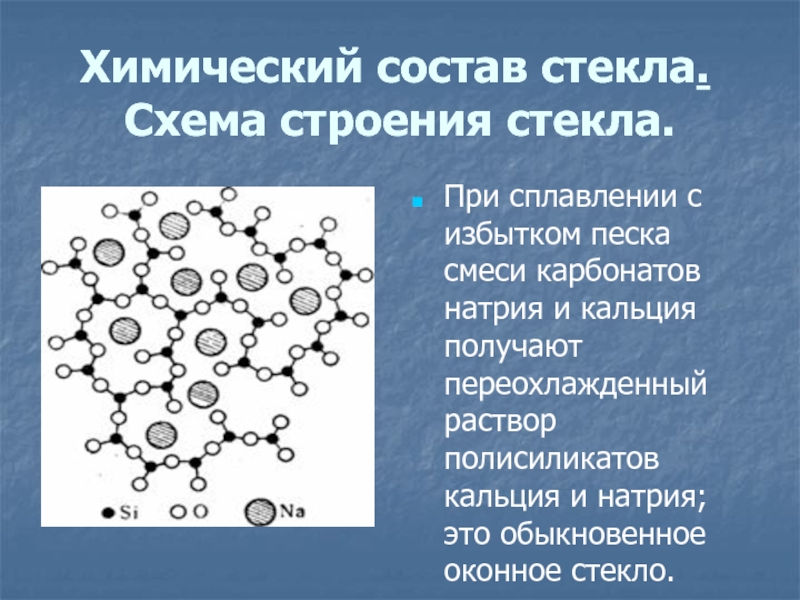 3, которые делают его идеальным материалом для использования в лаборатории.
3, которые делают его идеальным материалом для использования в лаборатории.
Многие продукты DWK Life Sciences соответствуют другим стандартам, установленным для лабораторной посуды; например, стеклянные стаканы соответствуют ISO 3819, а мерные колбы соответствуют ISO 1042 и DIN 12664. Обычно в этих стандартах указывается не только тип стекла, но также детали размеров, объемная точность и допуски.
Химический состав
3.3 Расширяющееся боросиликатное стекло обладает очень высокой стойкостью к воздействию воды, кислот, растворов солей, галогенов и органических растворителей. Только плавиковая кислота, горячая концентрированная фосфорная кислота и сильные щелочные растворы вызывают заметную коррозию стекла. Нейтральное боросиликатное стекло (ASTM E-438, тип 1B) также обладает превосходными свойствами химической стойкости, что делает его идеальным для хранения или упаковки кислых, нейтральных и щелочных продуктов, а также растворов для инъекций. Известково-натриевое стекло (ASTM E-438, тип 2) менее химически стойкое, чем боросиликатное стекло, и обычно подходит для хранения сухих порошков и контейнеров для хранения обычных проб.
Различные типы стекла имеют следующий типичный химический состав (прибл. % по весу):
| Химический | 3.3 Боросиликатное расширительное стекло | 4.9 Боросиликатное расширительное стекло (прозрачное) | 7.8 Расширяющееся натрий-известковое стекло (янтарное) | 9.1 Расширяющееся натрий-известковое стекло (прозрачное) | |
|---|---|---|---|---|---|
| SiO2 | 80,60% | 75,00% | 70,00% | 67,00% | 69,00% |
| Б2О3 | 13,00% | 10,50% | 7,50% | 5,00% | 1,00% |
| Na2O | 4,00% | 5,00% | 6,50% | 12,00% | 13,00% |
| Al2O3 | 2,30% | 7,00% | 6,00% | 7,00% | 4,00% |
| СаО | — | 1,50% | 1,00% | 5,00% | |
| Fe2O3 | — | — | 1,00% | 2,00% | — |
| Тио2 | — | — | 5,00% | — | — |
| К2О | — | — | 1,00% | 1,00% | 3,00% |
| ВаО | — | — | 2,00% | 2,00% | |
| Мно2 | — | — | — | 5,00% | — |
| MgO | — | — | — | — | 3,00% |
Физические свойства и химические данные для стекла
Гидролитическая стойкость
Для многих применений важно, чтобы лабораторная посуда обладала превосходной гидролитической стойкостью; например во время процедур паровой стерилизации, когда многократное воздействие водяного пара при высокой температуре может привести к выщелачиванию ионов щелочи (Na+). Боросиликатное стекло имеет относительно низкое содержание оксида щелочного металла и, следовательно, высокую стойкость к воздействию воды.
Боросиликатное стекло имеет относительно низкое содержание оксида щелочного металла и, следовательно, высокую стойкость к воздействию воды.
Кислотостойкость
Стекла с высоким процентным содержанием диоксида кремния (SiO2) менее подвержены воздействию кислот. 3.3 Расширяющееся боросиликатное стекло содержит более 80% диоксида кремния и поэтому обладает исключительной устойчивостью к кислотам (за исключением горячей концентрированной фосфорной кислоты и плавиковой кислоты). Стекло разделено на 4 класса кислотостойкости, а боросиликатное стекло соответствует классу S1 по DIN 12116 и соответствует требованиям ISO 1776.
Щелочестойкость
Щелочные растворы воздействуют на все стекла, а боросиликатное стекло можно классифицировать как умеренно стойкое. Щелочестойкость боросиликатного стекла соответствует требованиям класса A2 согласно ISO 695 и DIN 52322.
Более подробная информация о физических и химических свойствах стекла приведена в следующей таблице.
| 3.3 Боросиликатное расширительное стекло | 4.9 Боросиликатное расширительное стекло (прозрачное) | 5.4 Расширяющее боросиликатное стекло (янтарное) | 7.8 Расширяющее натриево-известковое стекло (янтарное) | 9.1 Расширяющее натриево-известковое стекло (прозрачное) | 3,3 | 4,9 | 5,4 | 7,8 | 9.1 |
|---|---|---|---|---|---|
| Рабочая точка °C | 1252 | 1160 | 1165 | 1050 | 1040 |
| Точка размягчения° C | 821 | 785 | 770 | 720 | 720 |
| Точка отжига ° C | 565 | 565 | 560 | 540 | 530 |
| Температура превращения ° C | 525 | 565 | 550 | 535 | 525 |
| Плотность при 25° Сг/см-3 | 2,23 | 2,34 | 2,42 | 2,5 | 2,5 |
| Гидролитическая стойкость | |||||
Согл. по ИСО 719 по ИСО 719 | Класс HGB 1 | Класс HGB 1 | Класс HGB 1 | Класс HGB 2 | Класс HGB 3 |
| Согл. к ЕР | Тип 1 | Тип 1 | Тип 1 | Тип 111 | Тип 111 |
| Согл. к USP | Тип 1 | Тип 1 | Тип 1 | Тип 111 | Тип 111 |
| Кислотостойкость (DIN 12116) | Класс S1 | Класс S1 | Класс S1 | Класс S2 | Класс S1 |
| Щелочестойкость (ISO 695) | Класс А2 | Класс А2 | Класс А2 | Класс А2 | Класс А2 |
Термостойкость
3.3 Расширяющееся боросиликатное стекло, такое как Pyrex ® , обладает превосходными термическими свойствами как при высоких, так и при низких температурах. Максимальная рекомендуемая рабочая температура для лабораторной посуды 3. 3 из расширяющегося боросиликатного стекла составляет 500°C (только на короткий период времени). Особое внимание следует уделить при температуре выше 150°C, чтобы обеспечить медленное и равномерное нагревание и охлаждение. 3.3 Расширяющееся боросиликатное стекло также отлично работает при более низких температурах и может выдерживать условия примерно до -192°C, что делает его пригодным для использования с жидким азотом. При обычном лабораторном использовании температура -70°C легко поддерживается в течение длительных периодов времени. Опять же, следует соблюдать особую осторожность, чтобы избежать резких изменений температуры, и охлаждение должно осуществляться медленным равномерным образом.
Особое внимание следует уделить при температуре выше 150°C, чтобы обеспечить медленное и равномерное нагревание и охлаждение. 3.3 Расширяющееся боросиликатное стекло также отлично работает при более низких температурах и может выдерживать условия примерно до -192°C, что делает его пригодным для использования с жидким азотом. При обычном лабораторном использовании температура -70°C легко поддерживается в течение длительных периодов времени. Опять же, следует соблюдать особую осторожность, чтобы избежать резких изменений температуры, и охлаждение должно осуществляться медленным равномерным образом.
Оптические данные
Боросиликатное стекло Pyrex ® прозрачно и бесцветно на вид и, таким образом, пропускает свет в видимом диапазоне спектра. Это качество делает его идеальным для работ, связанных с фотохимическими реакциями, например, хлорированием. График (ниже) показывает степень пропускания света в зависимости от длины волны в ультрафиолетовой, видимой и инфракрасной областях спектра. Для большинства стеклянной посуды, представленной в нашем каталоге, толщина стекла составляет 2 – 5 мм.
Для большинства стеклянной посуды, представленной в нашем каталоге, толщина стекла составляет 2 – 5 мм.
Посуда из стекла Pyrex
® с янтарным покрытием
Несколько продуктов марки Pyrex ® , включая лабораторные бутыли со средами и мерные колбы, доступны из стекла с янтарным покрытием. Стеклянная посуда покрыта на внешней поверхности коричневым диффузионным цветом, что приводит к сильному поглощению в коротковолновой области до 500 нм. Эта функция особенно полезна при работе с реагентами, чувствительными к свету.
Центрифужные пробирки
DWK Life Sciences может поставить ряд Pyrex 9Центрифужные пробирки 0011® и Quickfit ® . Мы рекомендуем максимальную относительную центробежную силу (RCF), которой они могут подвергаться, в информации о конкретном продукте. Перед центрифугированием важно рассчитать фактические значения относительной центробежной силы, которые будут получены. Это можно быстро определить, используя следующую номограмму.
стеклянных материалов | Текущий
Кремнезем, более известный как стекло, является универсальным материалом, используемым во множестве промышленных процессов, от катализа и фильтрации до хроматографии и нанопроизводства. Тем не менее, несмотря на его повсеместное распространение в лабораториях и чистых помещениях, на удивление мало известно о взаимодействии поверхности кремнезема с водой на молекулярном уровне.
«То, как вода взаимодействует с поверхностью, влияет на многие процессы», — сказал Сонги Хан, профессор химии из Калифорнийского университета в Санта-Барбаре и автор недавней статьи в Proceedings of the National Academy of Sciences. Она объяснила, что во многих случаях ученые и инженеры интуитивно понимают потенциальные взаимодействия между кремнеземом и водой и разрабатывают оборудование, эксперименты и процессы на основе эмпирических данных. Но механистическое понимание того, как химическая топология поверхности кремнезема изменяет структуру воды на поверхности, могло бы привести к рациональному построению этих процессов.
Для многих людей стекло — это стекло, и оно напоминает прозрачный, твердый, гладкий, однородный на вид материал, который мы используем для окон или посуды. Однако на более глубоком уровне то, что мы называем «стеклом», на самом деле является более сложным материалом, который может содержать различные химические свойства с широким диапазоном распределения.
«Стекло — это материал, с которым мы все знакомы, но многие люди, вероятно, не знают, что это то, что мы бы назвали химически гетерогенной поверхностью», — сказал аспирант-исследователь Алекс Шредер, ведущий автор статьи PNAS. .
По его словам, существует два различных типа химических групп, входящих в состав стеклянных поверхностей: силанольные (SiOH) группы, которые обычно являются гидрофильными (водолюбивыми), и силоксановые (SiOHSi) группы, которые обычно обладают водоотталкивающими свойствами. «Мы показываем, — сказал Шрейдер, — что то, как вы размещаете эти два типа химических веществ на поверхности, сильно влияет на то, как вода взаимодействует с поверхностью, что, в свою очередь, влияет на физические наблюдаемые явления, такие как то, как вода распространяется по поверхности. стекло.»
стекло.»
В некоторых процессах, таких как катализ, например, диоксид кремния (он же диоксид кремния или SiO 2 ) в виде беловатого порошка используется как носитель — катализатор прикрепляется к зернам порошка, которые в свою очередь увлекают его в процесс. Хотя кремнезем не участвует непосредственно в катализе, молекулярный состав поверхности зерен кремнезема может влиять на его эффективность, если химическая группа является преимущественно гидрофильной или гидрофобной. Исследователи обнаружили, что если кремнезем имеет тенденцию иметь гидрофильные силанольные группы на своей поверхности, он притягивает молекулы воды, фактически образуя «мягкий барьер» из молекул воды, который реагенты должны будут преодолеть, чтобы каким-то образом проникнуть, чтобы продолжить желаемый процесс или реакцию. .
«Всегда есть динамика, и молекулы воды должны поменяться местами, и поэтому это сложно», — сказал профессор химической инженерии UCSB Джейкоб Исраэлачвили, чей аппарат поверхностных сил (SFA) измерял силы взаимодействия между поверхностями кремнезема через воду. «Вы должны разорвать одну связь, чтобы образовалась другая связь. А это может занять время».
«Вы должны разорвать одну связь, чтобы образовалась другая связь. А это может занять время».
Не только наличие силанольных групп может повлиять на адгезию воды к поверхностям из диоксида кремния. Исследователи были озадачены нелинейным падением коэффициента диффузии поверхностной воды, измеренным прибором динамической ядерной поляризации Оверхаузера в лаборатории Хана, когда химический состав поверхности кремнезема изменился с гидрофобного на гидрофильный. Эта загадка впоследствии была решена профессором химического машиностроения UCSB Скоттом Шеллом и его аспирантом Джейкобом Монро, чье компьютерное моделирование показало, что относительное расположение силанольных и силоксановых групп на поверхности также влияет на адгезию воды.
«Если у вас есть одинаковая доля групп, любящих воду, и групп, не любящих воду, просто переставив их в пространстве, вы можете значительно изменить подвижность воды», — сказал Хан.
Каталитические процессы — не единственное, что можно улучшить с помощью молекулярного понимания адгезии диоксида кремния и воды. Фильтрация и хроматография также могут быть улучшены.
Фильтрация и хроматография также могут быть улучшены.
«Это также важно в процедурах чистых помещений, нанопроизводстве и формировании микропроцессоров», — сказал Шрадер, который указал, что микропроцессоры изготавливаются на подложках из кремниевых пластин с тонким слоем стекла, на которые накладываются схемы. «Важно понять, как реальная поверхность кремниевой пластины выглядит на химическом уровне, и как эти различные металлические слои, которые они наносят на нее, прилипают к ней и как они выглядят».
Все о натриево-известковом стекле – Состав и свойства – Передовые технические продукты
Возможно, вы слышали о натриево-известковом стекле, но что это такое?
По словам Томаса Нетта:
Что такое известково-натриевое стекло?
«Известково-натриевое стекло является наиболее часто производимым типом стекла, составляющим 90% всего производимого стекла. Производимый в течение сотен лет, он представляет собой базовую комбинацию кремнезема, соды и извести с множеством полезных свойств для применения в различных отраслях, включая производство потребительских товаров, упаковку и научный сектор. Известково-натриевое стекло часто противопоставляют его двоюродному брату, боросиликатному стеклу, которое более подробно обсуждается здесь .
Известково-натриевое стекло часто противопоставляют его двоюродному брату, боросиликатному стеклу, которое более подробно обсуждается здесь .
«Вот какие области охватит это руководство:
- Состав
- Свойства
- Таблица свойств
- Применение
Состав натриево-известкового стекла
«Известково-натриевое стекло изготавливается в основном из трех основных компонентов. Первый материал — кремнезем, или диоксид кремния, который составляет 70% готового продукта. Еще 15% состоит из соды или оксида натрия, который снижает температуру плавления кремнезема, а известь, также известная как оксид кальция, составляет еще 9%.% действовать как стабилизатор. Остальные 6% составляют микроэлементы.
Свойства известково-натриевого стекла
«Известково-натриевое стекло обладает несколькими свойствами, которые делают его полезным в качестве стекла для общих и более специфических применений.
» Это дешево. Известково-натриевое стекло дешевле, чем другое стекло с более специфическими свойствами, например боросиликатное или оптическое стекло.
Известково-натриевое стекло дешевле, чем другое стекло с более специфическими свойствами, например боросиликатное или оптическое стекло.
» Химически стабилен. Атомы в натриево-кальциевом стекле имеют прочные атомные связи и тесно связаны друг с другом, что затрудняет воздействие других веществ на его структуру и коррозию стекла. Это делает его подходящим для использования с химическими веществами, особенно если его закалить для повышения его устойчивости к тепловому удару. Однако известково-натриевое стекло не полностью невосприимчиво к химическому износу, и другие более специализированные стекла могут быть более устойчивыми.
» Тяжело. Известково-натриевое стекло имеет твердость 6–7 по шкале Мооса, которая показывает, насколько материал устойчив к истиранию. Этот наивысший балл по этой шкале равен десяти и включает в себя такие материалы, как алмаз. Однако известково-натриевое стекло также можно закалить с помощью тепла или химикатов, чтобы оно стало в три раза прочнее. Химическая закалка придает ему большую механическую прочность, делая его более твердым и устойчивым к царапинам. Термоупрочнение также придает стеклу механическую прочность, а также делает его более устойчивым к резким перепадам температуры.
Химическая закалка придает ему большую механическую прочность, делая его более твердым и устойчивым к царапинам. Термоупрочнение также придает стеклу механическую прочность, а также делает его более устойчивым к резким перепадам температуры.
» Работает. Благодаря содержанию соды и извести в натриево-кальциевом стекле его можно многократно размягчать и размягчать без потери качества. Этот атрибут делает его хорошим материалом для вторичной переработки.
» Уязвим к тепловым ударам. Внезапные перепады температуры могут привести к разрушению известково-натриевого стекла. Это можно уменьшить путем термической закалки, которая придает этому материалу дополнительную прочность.
» Это электрический изолятор. Стекло плохо пропускает электричество, так как имеет высокое удельное сопротивление и низкую диэлектрическую проницаемость. Это делает его полезным для изоляции электротехнических изделий.
“ Пропускает видимый свет. Показатель преломления натриево-кальциевого стекла составляет примерно 1,5, что означает, что отражается только около 4% падающего на него света. Остальная часть проходит, что делает его отличным материалом для приложений, где важно светопропускание.
Показатель преломления натриево-кальциевого стекла составляет примерно 1,5, что означает, что отражается только около 4% падающего на него света. Остальная часть проходит, что делает его отличным материалом для приложений, где важно светопропускание.
Таблица свойств известково-натриевого стекла
«В приведенной ниже таблице более подробно описаны механические, термические, оптические, химические и электрические свойства известково-натриевого стекла. Ниже описаны класс свойства, само свойство, его измерение для известково-натриевого стекла и объяснение того, что измеряет свойство. Па — это сокращение от паскалей, единицы давления, а мкОм·см — это микроомы на сантиметр.
Таблица: Свойства известково-натриевого стекла
| Класс свойства | Свойство | Измерение | Пояснение | ||
| Термический/механический | Удельный вес | 2483 г/ см 3 | Вес на единицу объема | ||
| 0094 | Плотность | 2,44 г/см 3 | Масса единицы объема | ||
| Коэффициент Пуассона | . 22 22 | Насколько материал растягивается в одном направлении и сужается в другом при втягивании два разных направления | |||
| Модуль упругости | 7,2 x 1010 Па | Жесткость материала | |||
| 3,0 x 1010 Па | Степень сдвига, которую может выдержать материал | ||||
| Объемный модуль упругости | 4,3 x 1010 Па | Насколько материал устойчив к сжатию | |||
| Коэффициент теплового расширения | 8,6 x 10-6/ градусов C | Насколько изменяется объем материала при нагревании или охлаждении | |||
| Температура размягчения | 726 C/1340 F | Температура, при которой материал оседает под собственным весом | |||
| Точка отжига | 546 C/1015 F | Температура, при которой остаточное напряжение в материале снижается в течение нескольких минут | |||
| Точка деформации | 514 C/957 F | Температура, при которой остаточное напряжение в материале уменьшается в течение нескольких часов | |||
| Оптический | Показатель преломления | 1,523 (если I=435) или 1,513 (если I=645) | Измерение того, сколько света проходит через материал вместо отражение | ||
| Химическая | Гидролитическая стойкость | Класс 3 | Вероятность загрязнения материала химическими веществами при контакте с ним (химическая стойкость) | ||
| Электрические | Di электрическая постоянная при 20 градусах C (68 F) | 7,75 | Степень воздействия магнитного поля на материал | ||
| Удельное сопротивление | 7,94 x 1017 – 7,94 x 1018 мкОм·см 9009 8 | Насколько хорошо материал сопротивляется электропроводности |
Применение натриево-известкового стекла
«Из-за своей популярности и распространенности натриево-известковое стекло можно найти в самых разных отраслях промышленности.

